Produto hospitalar apresentou impurezas e medicamentos de uso em exames perderam autorização da agência
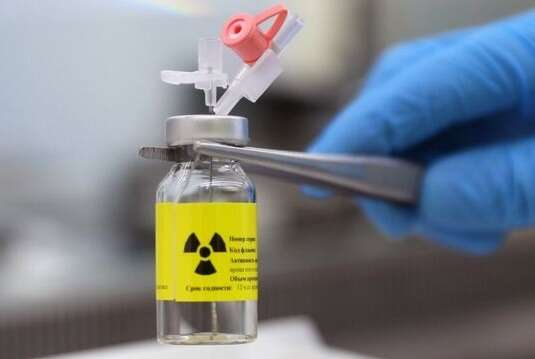
A Anvisa (Agência Nacional de Vigilância Sanitária) determinou, nesta segunda-feira (6), o recolhimento da Glicose 25% Solução Injetável, produzida pela empresa Samtec Biotecnologia Ltda. O lote afetado tem validade até 31 de julho de 2026. A decisão inclui a suspensão imediata da comercialização, distribuição e uso do produto.
A Anvisa determinou o recolhimento da Glicose 25% Solução Injetável, produzida pela Samtec Biotecnologia, após a identificação de material escuro no líquido pela Prefeitura de Joinville. O lote afetado tem validade até julho de 2026, e sua comercialização, distribuição e uso foram suspensos imediatamente.Além disso, a agência suspendeu a importação de 11 radiofármacos fabricados pelos Laboratórios Bacon S.A.I.C., da Argentina, após inspeção detectar falhas nas Boas Práticas de Fabricação. Os medicamentos são utilizados em procedimentos de medicina nuclear para diagnóstico e tratamento de diversas doenças.
A medida foi tomada após a Prefeitura de Joinville (SC) identificar desvio de qualidade no medicamento, que apresentou material escuro visível no líquido. A glicose injetável é utilizada em hospitais e pronto-atendimentos para tratar hipoglicemia (queda de açúcar no sangue), além de servir como fonte de energia intravenosa para pacientes debilitados ou impossibilitados de se alimentar.
A agência também suspendeu a importação de 11 medicamentos radiofármacos fabricados pelos Laboratórios Bacon S.A.I.C., da Argentina. O problema foi detectado após inspeção realizada em setembro que encontrou falhas nas BPF (Boas Práticas de Fabricação) de medicamentos estéreis em pó liofilizado, processo que remove a água para garantir a conservação.
Os produtos suspensos são usados em procedimentos de medicina nuclear, como diagnóstico de doenças cardíacas, neurológicas, renais e em tratamentos oncológicos. A lista inclui:
Neurobac Radiofarma, Ciprobac Radiofarma, Cloreto de Estanho Radiofarma, Disida Radiofarma, MAA (macroagregado de albumina) Radiofarma, Pirofosfato Radiofarma, Linfofast Radiofarma, Fitato de Sódio Radiofarma, DTPA (ácido dietilenotriaminopentacético) Radiofarma, Osteobac Radiofarma e Sestamibi Radiofarma.
Segundo a Anvisa, as BPF devem ser seguidas rigorosamente na fabricação de medicamentos estéreis, garantindo que os produtos estejam livres de microrganismos e seguros para uso clínico.
Receba as principais notícias do Estado pelo Whats. Clique aqui para acessar o canal do Campo Grande News e siga nossas redes sociais.